
La structure et les principes de base de la tomographie par cohérence optique.
Tomographie par cohérence optiqueest basé sur le principe de l'interféromètre, utilise une lumière cohérente faible dans le proche infrarouge pour irradier le tissu à tester et génère des interférences basées sur la cohérence de la lumière. Il utilise la technologie de détection superhétérodyne pour mesurer l'intensité de la lumière réfléchie pour l'imagerie des tissus superficiels. . Le système OCT est composé d'une source lumineuse à faible cohérence, d'un interféromètre de Michelson à fibre optique et d'un système de détection photoélectrique.
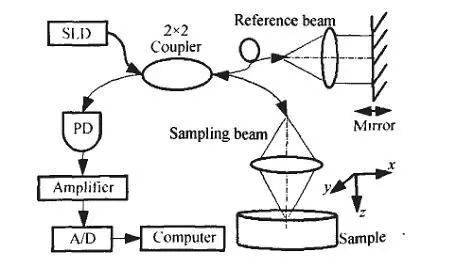
Le cœur de l'OCT est l'interféromètre de Michelson à fibre. La lumière émise par la diode de superluminescence (SLD) à source de lumière à faible cohérence est couplée dans la fibre monomode et est divisée en deux voies par le coupleur de fibre 2 × 2. Une façon est la lumière de référence qui est collimatée par la lentille et renvoyée par le miroir plan. ; L'autre est le faisceau d'échantillonnage focalisé par la lentille sur l'échantillon testé.
La lumière de référence renvoyée par le réflecteur et la lumière rétrodiffusée de l'échantillon sous test se confondent sur le détecteur. Lorsque la différence de chemin optique entre les deux se situe dans la longueur de cohérence de la source lumineuse, des interférences se produisent. Le signal de sortie du détecteur reflète la rétrodiffusion du milieu. Vers l'intensité de diffusion.
Scannez le miroir et enregistrez sa position spatiale, de sorte que la lumière de référence interfère avec la lumière rétrodiffusée à partir de différentes profondeurs dans le milieu. Selon la position du miroir et l'intensité du signal d'interférence correspondant, les données de mesure de différentes profondeurs (direction z) de l'échantillon sont obtenues. Puis combiné avec le balayage du faisceau d'échantillonnage dans le plan x-y, le résultat est traité par l'ordinateur pour obtenir les informations de structure tridimensionnelle de l'échantillon.
Le développement de la technologie d'imagerie OCT
Avec l'application généralisée des ultrasons dans le domaine de l'ophtalmologie, les gens espèrent développer une méthode de détection à plus haute résolution. L'émergence du biomicroscope à ultrasons (UBM) répond dans une certaine mesure à cette exigence. Il peut effectuer une imagerie haute résolution du segment antérieur en utilisant des ondes sonores à plus haute fréquence. Cependant, en raison de l'atténuation rapide des ondes sonores à haute fréquence dans les tissus biologiques, sa profondeur de détection est limitée dans une certaine mesure. Si des ondes lumineuses sont utilisées à la place des ondes sonores, les défauts peuvent-ils être compensés ?
En 1987, Takada et al. développé une méthode d'interférométrie optique à faible cohérence, qui a été développée en une méthode de mesure optique à haute résolution avec le support de fibres optiques et de composants optoélectroniques ; Youngquist et al. a développé un réflectomètre optique cohérent dont la source lumineuse est une super diode électroluminescente directement couplée à une fibre optique. Un bras de l'instrument contenant un miroir de référence est situé à l'intérieur, tandis que la fibre optique de l'autre bras est connectée à un dispositif semblable à une caméra. Ceux-ci ont jeté les bases théoriques et techniques de l'émergence de l'OCT.
En 1991, David Huang, un scientifique chinois du MIT, a utilisé l'OCT développé pour mesurer la rétine et les artères coronaires isolées. Parce que l'OCT a une haute résolution sans précédent, similaire à la biopsie optique, il a été rapidement développé pour la mesure et l'imagerie des tissus biologiques.
En raison des caractéristiques optiques de l'œil, la technologie OCT se développe le plus rapidement dans les applications cliniques en ophtalmologie. Avant 1995, des scientifiques tels que Huang utilisaient l'OCT pour mesurer et imager des tissus tels que la rétine, la cornée, la chambre antérieure et l'iris des yeux humains in vitro et in vivo, améliorant continuellement la technologie OCT. Après plusieurs années d'amélioration, le système OCT a été encore amélioré et développé en un outil de détection cliniquement pratique, transformé en un instrument commercial, et a finalement confirmé sa supériorité dans l'imagerie du fond d'œil et de la rétine. L'OCT a été officiellement utilisé dans les cliniques d'ophtalmologie en 1995.
En 1997, l'OCT a été progressivement utilisé dans les examens dermatologiques, digestifs, urinaires et cardiovasculaires. L'OCT de l'œsophage, de l'appareil gastro-intestinal et urinaire et l'OCT cardiovasculaire sont tous des examens invasifs, similaires aux endoscopes et aux cathéters, mais avec une résolution plus élevée et peuvent observer des ultrastructures. L'OCT cutané est une inspection par contact, et l'ultrastructure peut également être observée.
L'OCT initial utilisé dans la pratique clinique est l'OCT1, qui est composé d'une console et d'une console d'alimentation. La console comprend un ordinateur OCT, un moniteur OCT, un panneau de commande et un écran de surveillance ; la centrale électrique comprend un système d'observation du fond d'œil et un système de contrôle de la lumière d'interférence. Étant donné que la console et la plate-forme d'alimentation sont des appareils relativement indépendants et que les deux sont reliés par des fils, l'instrument a un plus grand volume et un plus grand espace.
Le programme d'analyse d'OCT1 est divisé en traitement d'image et mesure d'image. Le traitement d'image comprend la normalisation d'image, l'étalonnage d'image, l'étalonnage et la normalisation d'image, le lissage gaussien d'image, le lissage médian d'image ; les procédures de mesure d'image sont moindres, seules la mesure de l'épaisseur rétinienne et la mesure de l'épaisseur de la couche de fibres nerveuses rétiniennes. Cependant, comme OCT1 a moins de procédures de numérisation et de procédures d'analyse, il a été rapidement remplacé par OCT2.
OCT2 est formé par une mise à niveau logicielle sur la base d'OCT1. Il existe également des instruments qui combinent la console et la table de puissance en un seul pour former un instrument OCT2. Cet instrument réduit le moniteur d'image et observe l'image OCT et surveille la position de numérisation du patient sur le même écran d'ordinateur, mais le fonctionnement est le même que OCT1 Similaire, il est actionné manuellement sur le panneau de commande.
L'apparition d'OCT3 en 2002 a marqué une nouvelle étape de la technologie OCT. En plus de l'interface de fonctionnement plus conviviale d'OCT3, toutes les opérations peuvent être effectuées sur l'ordinateur avec la souris, et ses programmes de numérisation et d'analyse deviennent de plus en plus parfaits. Plus important encore, la résolution d'OCT3 est plus élevée, sa résolution axiale est de ≤10 μm et sa résolution latérale est de 20 μm. Le nombre d'échantillons axiaux acquis par OCT3 est passé de 128 à 768 dans le 1 A-scan original. Par conséquent, l'intégrale d'OCT3 est passée de 131 072 à 786 432, et la structure hiérarchique de l'image en coupe transversale du tissu numérisé est plus claire.
Copyright @ 2020 Shenzhen Box Optronics Technology Co., Ltd. - Chine Modules à fibre optique, fabricants de lasers couplés à fibre, fournisseurs de composants laser Tous droits réservés.